LA REVERSIÓN DE LA DIABETES (una realidad)
La diabetes, ¿enfermedad progresiva?
Actualmente se ha acumulado suficiente evidencia científica para cuestionar las hipótesis que promovieron la DM2 como una enfermedad crónica, inevitablemente progresiva e incurable. El concepto de la remisión de la DM2 ha surgido a finales del siglo 20 y se está desarrollando cada vez más en los últimos años. Tres enfoques no farmacológicos han demostrado altas tasas de reversión o remisión de DM2, al menos temporalmente: cirugía bariátrica 1, dietas muy bajas en calorías (VLCD) 2,3 y cetosis nutricional lograda a través de la restricción de hidratos de carbono en la dieta. 4,5,6,7
A partir de los datos esperanzadores de estudios con cirugía bariátrica 1 y otros que han conseguido reversión de la DM2 sin tenerlo como objetivo principal 8, se han realizado varios estudios para la remisión de la DM2. En Reino Unido, en condiciones de atención primaria, se han realizado la serie de estudios DiRECT 2,3,9, enfocados en la pérdida de peso utilizando una dieta hipocalórica. Se trata de un estudio, diseñado para evaluar si la reducción de peso, podría producir una remisión sostenida de la DM2. En este estudio realizado en 49 prácticas de atención primaria en Escocia e Inglaterra, se registró a los 12 meses una pérdida de 15 o más kg de peso en 24 % de los participantes en el grupo de intervención y en ningún participante en el grupo control (P < 0,0001). La remisión de la DM2 se logró en 46 % de los participantes en el grupo de intervención y en 4 % de los participantes en el grupo control [odds ratio 19,7; IC (95 %) 7,8 – 49,8; P < 0,0001]. Además, se demostró una clara correlación entre la tasa de remisión y la pérdida de peso, aunque no todos los sujetos que revirtieron la diabetes necesariamente bajaron mucho peso. El programa DiRECT mantuvo remisiones a los 24 meses para más de un tercio de las personas con DM2 9. La remisión sostenida se relacionó con el mantenimiento de la pérdida de peso alcanzada.
Reversión a través de cambio metabólico (cetosis nutricional)
En serie de publicaciones de un grupo de intervención telemática estadounidense se demuestran varios beneficios de la reversión de la DM2 usando cetosis nutricional sin restricción calórica intencionada 4,5,6,7 : mejoría de indicadores de salud metabólica 5,6 y cardiovascular como son la obesidad, glucemia basal, HbA1c, tensión arterial, dislipemia, filtrado glomerular (función renal), reactantes de la fase aguda (inflamación), indicadores de esteatosis hepática (hígado graso)13, 14, sostenibilidad a lo largo de, por lo menos, 2 años5 y todo esto asociado a retirada de medicación para la DM2, para la hipertensión arterial y otras comorbilidades.
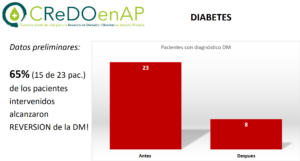
En un estudio piloto realizado por un servidor, se ha obtenido reversión de diabetes en casi 65% de un grupo de pacientes (datos propios), seleccionados para cumplir criterios de hiperinsulinismo. Estos criterios de selección coinciden con el fenotipo más común dentro de la diabetes, la diabetes, asociada al sobrepeso progresivo o a la obesidad.
Consenso sobre reversión y remisión
Un grupo de expertos de consenso de ADA ha elaborado y consensuado criterios y definiciones de los términos reversión, remisión parcial, completa y prolongada de la DM 15. Reversión de la Diabetes se consideraría alcanzar niveles glucémicos (glucemia basal y HbA1c) por debajo de los niveles mínimos suficientes para el diagnóstico de DM, o sea, glucemia basal menos de 126 mg/dl y HbA1c menos de 6,5 %. Se ha establecido como Remisión parcial mantener durante 1 año niveles de glucemia basal/HbA1c compatibles con Reversión. Remisión completa se considera glucemia basal correspondiente a niveles normales (< 100mg/dl) y de HbA1c < 5,9. Remisión prolongada se considera cuando la completa persiste más de 5 años. Para cumplir criterios de remisión es necesaria la ausencia de cualquier terapia farmacológica o de procedimientos, como por ejemplo podrían ser los ajustes de banda gástrica.
BIBLIOGRAFIA
1. Sjöström L, Peltonen M, Jacobson P, Ahlin S, Andersson-Assarsson J, Anveden Å, et al. Association of bariatric surgery with long-term remission of type 2 diabetes and with microvascular and macrovascular complications. JAMA - Journal of the American Medical Association. 2014;311(22):2297–304.
2. Lean MEJ, Leslie WS, Barnes AC, Brosnahan N, Thom G, McCombie L, et al. Primary care-led weight management for remission of type 2 diabetes (DiRECT): an open-label, cluster-randomised trial. The Lancet. 2018 Feb 10;391(10120):541–51.
3. Taylor R. Calorie restriction for long-term remission of type 2 diabetes. Clin Med J R Coll Physicians London. 2019;19(1):37–42.
4. Hallberg SJ, McKenzie AL, Williams PT, Bhanpuri NH, Peters AL, Campbell WW, et al. Effectiveness and Safety of a Novel Care Model for the Management of Type 2 Diabetes at 1 Year: An Open-Label, Non-Randomized, Controlled Study. Diabetes Therapy [Internet]. 2018;9(2):583–612. Available from: https://doi.org/10.1007/s13300-018-0373-9
5. Athinarayanan SJ, Adams RN, Hallberg SJ, McKenzie AL, Bhanpuri NH, Campbell WW, et al. Long-term effects of a novel continuous remote care intervention including nutritional ketosis for the management of type 2 diabetes: A 2-year nonrandomized clinical trial. Front Endocrinol (Lausanne). 2019;10(JUN).
6. McKenzie AL, Hallberg SJ, Creighton BC, Volk BM, Link TM, Abner MK, et al. A Novel Intervention Including Individualized Nutritional Recommendations Reduces Hemoglobin A1c Level, Medication Use, and Weight in Type 2 Diabetes. JMIR Diabetes. 2017;2(1):e5.
7. Unwin D, Delon C, Unwin J, Tobin S, Taylor R. What predicts drug-free type 2 diabetes remission? Insights from an 8-year general practice service evaluation of a lower carbohydrate diet with weight loss. BMJ Nutr Prev Health. 2023 Jan 2;e000544.
8. Wing RR, Bolin P, Brancati FL, Bray GA, Clark JM, Coday M, et al. Cardiovascular effects of intensive lifestyle intervention in type 2 diabetes. N Engl J Med. 2013 Jul;369(2):145–54.
9. Lean MEJ, Leslie WS, Barnes AC, Brosnahan N, Thom G, McCombie L, et al. Durability of a primary care-led weight-management intervention for remission of type 2 diabetes: 2-year results of the DiRECT open-label, cluster-randomised trial. Lancet Diabetes Endocrinol. 2019;7(5):344–55.
10. Bhanpuri NH, Hallberg SJ, Williams PT, McKenzie AL, Ballard KD, Campbell WW, et al. Cardiovascular disease risk factor responses to a type 2 diabetes care model including nutritional ketosis induced by sustained carbohydrate restriction at 1 year: An open label, non-randomized, controlled study. Cardiovasc Diabetol [Internet]. 2018;17(1):1–16. Available from: https://doi.org/10.1186/s12933-018-0698-8
11. Unwin D, Unwin J, Crocombe D, Delon C, Guess N, Wong C. Renal function in patients following a low carbohydrate diet for type 2 diabetes. Curr Opin Endocrinol Diabetes Obes. 2021;Publish Ah.
12. Unwin DJ, Tobin SD, Murray SW, Delon C, Brady AJ. Substantial and sustained improvements in blood pressure, weight and lipid profiles from a carbohydrate restricted diet: An observational study of insulin resistant patients in primary care. Int J Environ Res Public Health. 2019;16(15).
13. Vilar-Gomez E, Athinarayanan SJ, Adams RN, Hallberg SJ, Bhanpuri NH, McKenzie AL, et al. Post hoc analyses of surrogate markers of non-alcoholic fatty liver disease (NAFLD) and liver fibrosis in patients with type 2 diabetes in a digitally supported continuous care intervention: An open-label, non-randomised controlled study. BMJ Open. 2019;9(2):1–12.
14. Dyńka D, Rodzeń Ł, Rodzeń M, Łojko D, Kraszewski S, Ibrahim A, et al. Beneficial Effects of the Ketogenic Diet on Nonalcoholic Fatty Liver Disease (NAFLD/MAFLD). J Clin Med [Internet]. 2024 Aug 17;13(16):4857. Available from: https://www.mdpi.com/2077-0383/13/16/4857
15. Riddle MC, Cefalu WT, Evans PH, Gerstein HC, Nauck MA, Oh WK, et al. Consensus report: Definition and interpretation of remission in type 2 diabetes. Diabetes Care. 2021 Oct 1;44(10):2438–44.